Risiko Meningkat, Investor Keluar dari Surat Utang Negara
21 jam yang lalu
Waktu baca 2 menit
Waktu baca 2 menit

Amerika Serikat Segera Terapkan Sanksi Baru kepada Iran
21 jam yang lalu
Waktu baca 2 menit
Waktu baca 2 menit

ASN Pionir Pindah ke IKN Dapat Tunjangan Khusus
21 jam yang lalu
Waktu baca 2 menit
Waktu baca 2 menit

Menteri Pertahanan AS dan Tiongkok Bahas Keamanan Regional dan Global
21 jam yang lalu
Waktu baca 3 menit
Waktu baca 3 menit
-
01
-
02
Michael Douglas Minta Karakternya Mati di Film "Ant-Man" 2023
23 menit yang lalu
Waktu baca 1 menit -
03
Zayn Malik Berbagi Cerita Tentang Anak Perempuannya
33 menit yang lalu
Waktu baca 2 menit -
04
Ashanti Umumkan Kehamilan dan Pertunangannya dengan Nelly
43 menit yang lalu
Waktu baca 1 menit
-
01
Peta Jalan Pendidikan Belum Memiliki Arah yang Jelas
13-03-2021, 05:45 WIB
Waktu baca 3 menit -
02
Satu Buku Ditunggu oleh 90 Orang Setiap Tahun
25-03-2021, 06:14 WIB
Waktu baca 2 menit -
03
Dana KIP-Kuliah Membuat Mahasiswa Kurang Mampu Lebih Percaya Diri
20-03-2021, 06:26 WIB
Waktu baca 3 menit -
04
Birokrasi Wajib Mengaplikasikan Nilai-nilai Pancasila
29-03-2021, 06:33 WIB
Waktu baca 3 menit
Lihat Lainnya
Nasional
Terbaru di Nasional

BMKG Peringatkan Potensi Hujan Petir di Kubu Raya
3 jam yang lalu
Waktu baca 1 menit
Waktu baca 1 menit

BMKG Deteksi 383 Titik Panas di Kaltim
3 jam yang lalu
Waktu baca 2 menit
Waktu baca 2 menit

BMKG: Waspada Cuaca Ekstrem di Bengkulu Hingga Beberapa Hari ke Depan
3 jam yang lalu
Waktu baca 1 menit
Waktu baca 1 menit

Badan Geologi: Gunung Ruang Erupsi Eksplosif Beberapa Kali
4 jam yang lalu
Waktu baca 1 menit
Waktu baca 1 menit
Popular di Nasional

Semoga Tidak Terjadi Penumpukan Kendaraan, Menhub Sebut Salatiga Sampai Semarang Titik Krusial Arus Balik
12-04-2024, 06:00 WIB
Waktu baca 4 menit
Waktu baca 4 menit

1,5 Juta Kendaraan Tinggalkan Jabotabek pada Hari Raya Idul Fitri
11-04-2024, 14:30 WIB
Waktu baca 2 menit
Waktu baca 2 menit

Jangan Mbolos, Pemkot Semarang Ingatkan ASN Masuk Kerja Sesuai Jadwal Usai Lebaran
15-04-2024, 00:28 WIB
Waktu baca 1 menit
Waktu baca 1 menit

KSAL Halalbihalal dengan Prajurit di Mabesaldi Hari Pertama Kerja
16-04-2024, 15:45 WIB
Waktu baca 2 menit
Waktu baca 2 menit
Lihat Lainnya
Video Terbaru

Presiden Jokowi Akan Temui Pelajar dan Resmikan Papua Street Carnival

Diperiksa Selama 9 Jam, Panji Gumilang Belum Ditetapkan sebagai Tersangka

Tinggalkan Milan, Tonali Bergabung ke Newcastle

Kemendikbudristek Perkuat Pencegahan Korupsi Di Lingkungan Pendidikan
Lihat Lainnya
Infografis
Lihat Lainnya
Foto Terbaru

Pasokan Turun

Permintaan Meningkat

Halal Bihalal Pemerintah Kota Bogor

Wapres Gelar Halal Bihalal

Pemberantasan TPPU

Jawab Sejumlah Isu

JAKARTA KEMBALI MACET

Tribute to Black Brothers "Merajut Kebangsaan"

Konsumsi Tinggi

Pembangunan Pansela

IHSG Melemah

Ruas Jalan Depok Menuju Jakarta Padat
Lihat Lainnya
Mondial
Terbaru di Mondial

Filipina dan AS Gelar Latihan untuk Rebut Kembali Pulau
18 jam yang lalu
Waktu baca 3 menit
Waktu baca 3 menit

CSIS: Korut Batalkan Peluncuran Satelit Pengintai
18 jam yang lalu
Waktu baca 1 menit
Waktu baca 1 menit

Aung San Suu Kyi Jalani Tahanan Rumah
18 jam yang lalu
Waktu baca 3 menit
Waktu baca 3 menit

Gawat Dikhawatirkan Akan Meningkat, Rusia Diterjang Banjir akibatkan Lebih dari 13.500 Orang Dievakuasi
19 jam yang lalu
Waktu baca 1 menit
Waktu baca 1 menit
Popular di Mondial

Taipan Properti Vietnam Dijatuhi Hukuman Mati dalam Kasus Penipuan senilai $27 Miliar
11-04-2024, 20:05 WIB
Waktu baca 3 menit
Waktu baca 3 menit

Bankir Ternama India Memperingatkan The Fed akan Menunda Turunkan Suku Bunga hingga Pemilu AS pada November 2024
11-04-2024, 20:29 WIB
Waktu baca 2 menit
Waktu baca 2 menit
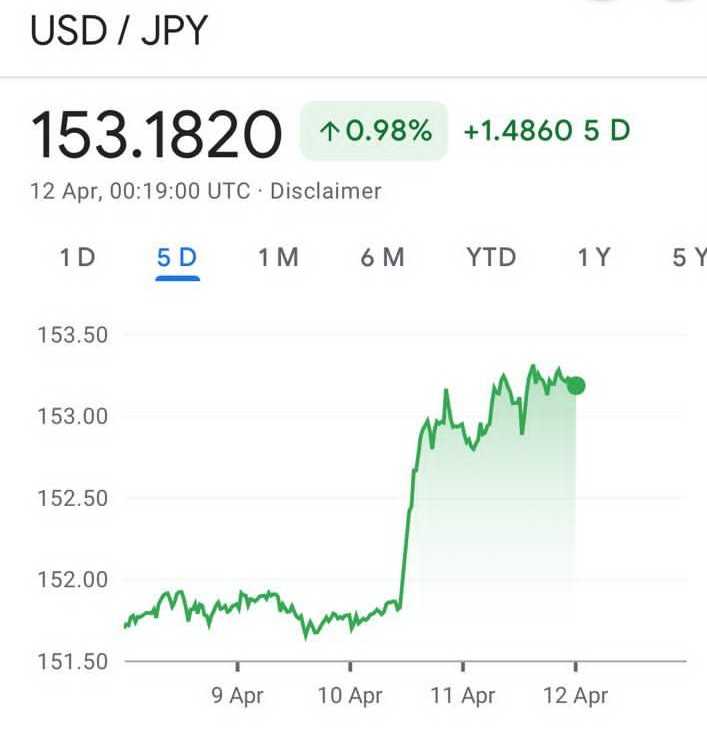
Yen Jatuh ke Titik Terendah dalam 34 Tahun Terakhir
12-04-2024, 10:33 WIB
Waktu baca 1 menit
Waktu baca 1 menit

Notre-Dame Segera Dibuka Kembali Pasca-Kebakaran 5 Tahun Lalu
13-04-2024, 15:26 WIB
Waktu baca 2 menit
Waktu baca 2 menit
 Muat Lainnya
Muat Lainnya